માનવ સંસાધન વિકાસ મંત્રાલય
IITGNના સંશોધકો પ્રોસ્ટેટ કેન્સરમાં સારવાર પ્રતિકારને દૂર કરવા માટે વધુ સ્માર્ટ દવાઓ વિકસાવી રહ્યા છે
ટીમે મોલેક્યુલર તોડફોડ દ્વારા કેન્સરના અસ્તિત્વ ટકાવી રાખવાની યુક્તિઓને વિક્ષેપિત કરવા માટે 5n, એક સંભવિત પ્રોસ્ટેટ કેન્સર અવરોધક વિકસાવ્યું
આ પરમાણુ TLK1ને નિષ્ક્રિય કરે છે, જે પ્રોસ્ટેટ કેન્સર કોષોમાં ગાંઠની રીકવરી રોકવા માટે જરૂરી રિપેર પ્રોટીન છે, જે નવી હસ્તક્ષેપ વ્યૂહરચનાઓનો માર્ગ મોકળો કરે છે
प्रविष्टि तिथि:
28 MAY 2025 5:22PM by PIB Ahmedabad
કેન્સર ઘણીવાર અવિરત જૈવિક શસ્ત્ર સ્પર્ધામાં આપણી સારવારને પાછળ છોડી દે છે, પ્રતિકાર આપણે પ્રતિભાવ આપી શકીએ તેના કરતાં વધુ ઝડપથી વિકસિત થાય છે. પ્રોસ્ટેટ કેન્સર, જે વાર્ષિક 1.4 મિલિયનથી વધુ પુરુષોને અસર કરે છે. તે સામાન્ય રીતે ધીમી ગતિએ વધતા અને સારવાર કરી શકાય તેવા રોગ તરીકે શરૂ થાય છે. જો કે, કેન્સર કોષો ઉપચાર માટે પ્રતિકાર વિકસાવે ત્યારે તે જીવલેણ બની શકે છે. દાયકાઓથી, ડોકટરો ટેસ્ટોસ્ટેરોનને અવરોધવા માટે એન્ડ્રોજન ડિપ્રિવેશન થેરાપી (ADT) પર આધાર રાખે છે. એક હોર્મોન જે પ્રોસ્ટેટ ગાંઠોના વિકાસને બળતણ આપે છે. જ્યારે ADT ટેસ્ટોસ્ટેરોનના કેન્સરને અસરકારક રીતે ભૂખે મરાવે છે, ત્યારે ગાંઠ કોષોએ આ અવરોધને બાયપાસ કરવાની ચતુરાઈભરી રીતો શોધી કાઢી છે. જે ઓછા હોર્મોન સ્તર હોવા છતાં તેમની વૃદ્ધિને ફરીથી સક્રિય કરે છે. આ રોગના અદ્યતન, સારવાર-પ્રતિરોધક સ્વરૂપને મેટાસ્ટેટિક કાસ્ટ્રેશન-પ્રતિરોધક પ્રોસ્ટેટ કેન્સર (mCRPC) તરીકે ઓળખવામાં આવે છે અને તે દર વર્ષે વિશ્વભરમાં 375,000થી વધુ મૃત્યુ માટે જવાબદાર છે.
IIT ગાંધીનગરની કેન્સર કેમિકલ બાયોલોજી લેબની એક સંશોધન ટીમે તાજેતરમાં એક પરમાણુ ઓળખ્યું છે. જે કેન્સર કોષો દ્વારા પ્રમાણભૂત ઉપચારનો પ્રતિકાર કરવા માટે ઉપયોગમાં લેવાતી મુખ્ય અસ્તિત્વ પદ્ધતિને લક્ષ્ય બનાવે છે. "સામાન્ય રીતે, કેન્સર કોષો ટાઉસલ્ડ-લાઇક કાઇનેઝ 1 (TLK1) નામના પ્રોટીનને સક્રિય કરે છે, જે મોલેક્યુલર રિપેર ક્રૂની જેમ કાર્ય કરે છે," એવું અભ્યાસના લેખક અને IITGNના રસાયણશાસ્ત્ર વિભાગના પ્રોફેસર ડૉ. શિવપ્રિયા કિરુબાકરણે સમજાવ્યું હતું. "જ્યારે ADT જેવી ઉપચારો કેન્સર કોષોના DNA ને નુકસાન પહોંચાડે છે. ત્યારે TLK1 વિરામોને ઠીક કરવા માટે ઝંપલાવે છે, જેનાથી ગાંઠો ટકી રહે છે, ફેલાય છે અને mCRPCમાં વિકસિત થાય છે."
TLK1 અવરોધકોનો ઉપયોગ કરતી પરંપરાગત ઉપચાર પદ્ધતિઓ ફેનોથિયાઝિન તરીકે ઓળખાતા સંયોજનોના નાના વર્ગ સુધી મર્યાદિત રહી છે. શરૂઆતમાં એન્ટિસાઈકોટિક દવાઓ તરીકે વિકસાવવામાં આવી હતી, તેઓ પ્રોસ્ટેટ કેન્સર ઉપચારમાં મર્યાદિત વિશિષ્ટતા અને શક્તિ દર્શાવે છે અને અનિચ્છનીય આડઅસરો સાથે સંકળાયેલી છે. IITGN ટીમે વધુ સારી સલામતી અને અસરકારકતા સાથે અવરોધકોનો એક નવો વર્ગ બનાવીને આ અંતરને દૂર કરવાનો પ્રયાસ કર્યો હતો.
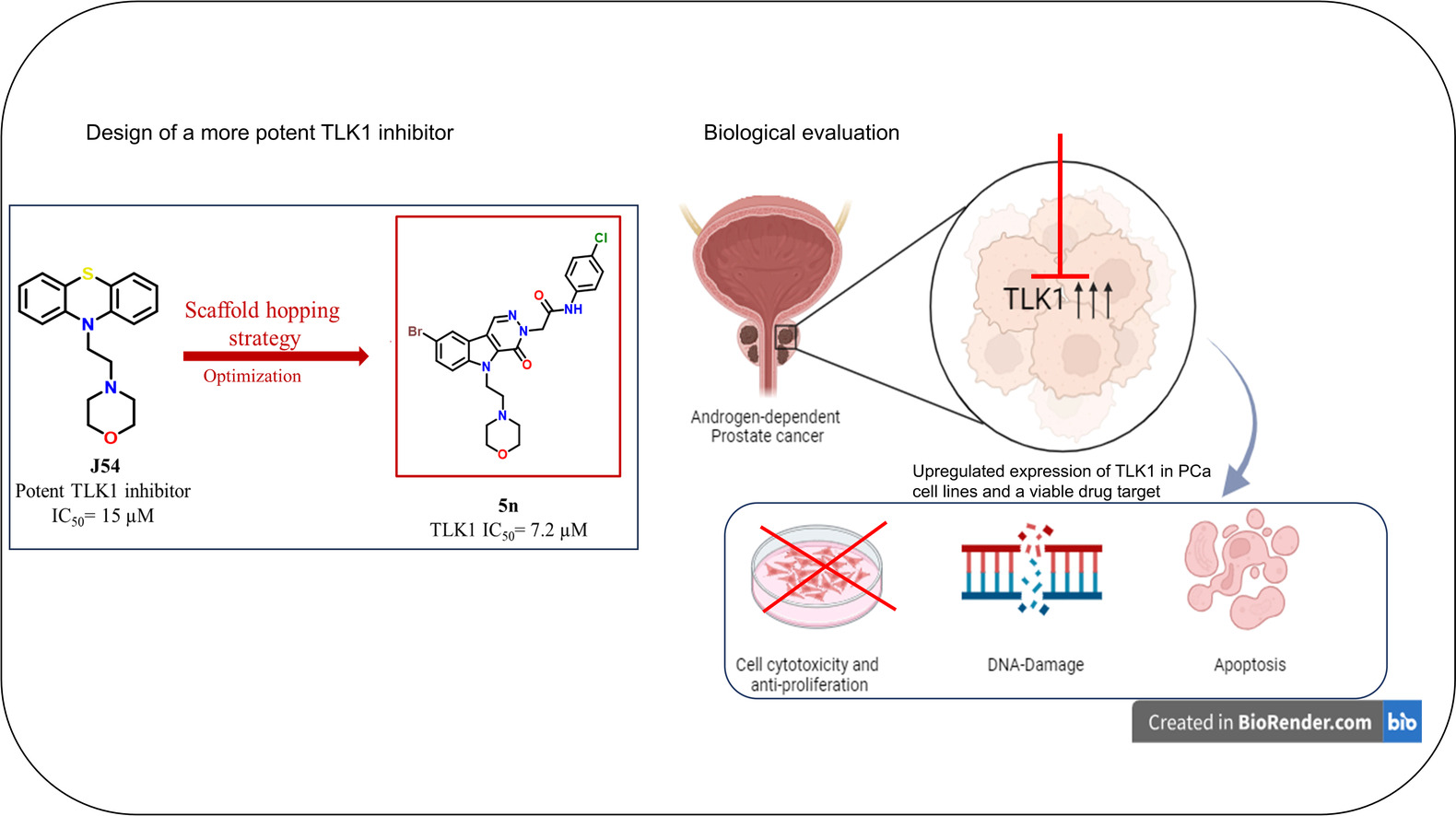
અભ્યાસના પ્રથમ લેખક અને IITGNના કેન્સર કેમિકલ બાયોલોજી લેબમાં પોસ્ટડોક્ટરલ ફેલો ડૉ. ડેલ્ના જોહ્ન્સને જણાવ્યું હતું કે "અમે અમારા ઇન-હાઉસ ડિઝાઇન કરેલા ફેનોથિયાઝિન-આધારિત TLK1 અવરોધક, J54ને સંશોધિત કરીને નવી દવાના પ્રકારો ડિઝાઇન કર્યા છે." J54 લેબના ભૂતપૂર્વ સંશોધકો દ્વારા વિકસાવવામાં આવ્યું હતું અને અગાઉના અભ્યાસોમાં mCRPC સામે અસરકારક કાર્યવાહી દર્શાવી છે. "અમે J54ના મુખ્ય માળખાને બદલ્યું અને TLK1 પ્રોટીન સાથે મજબૂત ક્રિયાપ્રતિક્રિયાઓ બનાવવા માટે સક્ષમ નવા અણુઓ બનાવવા માટે તેના અન્ય ભાગોને વ્યવસ્થિત રીતે સંશોધિત કર્યા હોવાનું પણ તેણીએ ઉમેર્યું હતું.
સંશોધન ટીમે અણુઓની બે શ્રેણીનું સંશ્લેષણ કર્યું અને તેમની જૈવિક પ્રવૃત્તિનું મૂલ્યાંકન કરવા માટે પ્રયોગોનો એક વ્યાપક સમૂહ કર્યો. ઇન વિટ્રો (ટેસ્ટ ટ્યુબ) પરીક્ષણોમાં, ઘણા સંયોજનોએ TLK1નું આશાસ્પદ અવરોધ દર્શાવ્યું, જેમાં એક પરમાણુ, 5n નામનો, સૌથી શક્તિશાળી તરીકે ઉભો રહ્યો. પરમાણુ 5n TLK1ને J54 કરતાં નોંધપાત્ર રીતે વધુ સારી રીતે અટકાવી શકે છે અને નિર્ણાયક રીતે, તેણે કોષના પ્રાથમિક ઊર્જા પરમાણુ, ATP સાથે સ્પર્ધા કર્યા વિના આમ કર્યું હતું. આ બિન-ATP-આધારિત પદ્ધતિ ખાતરી કરશે કે 5n સેલ્યુલર હોવા છતાં પણ TLK1 પ્રવૃત્તિને અવરોધિત કરી શકે છે. ATP વિપુલ પ્રમાણમાં છે. જેના કારણે ગાંઠ માટે તેને દૂર કરવાનું મુશ્કેલ બને છે. "J54ની મોર્ફોલિન-આધારિત સાઇડ ચેઇન, જે ઘણી દવાઓમાં એક સામાન્ય રાસાયણિક માળખું છે, તેને જાળવી રાખીને અને એમાઇડ લિંકર ઉમેરીને, અમારી ટીમે એક મોલેક્યુલર ડિકોય બનાવ્યું જે બાકીની સેલ્યુલર મશીનરીને ખલેલ પહોંચાડ્યા વિના પ્રોટીનના કાર્યને અક્ષમ કરે છે," અભ્યાસના વરિષ્ઠ લેખક અને IITGNના જૈવિક વિજ્ઞાન અને એન્જિનિયરિંગ વિભાગના એસોસિયેટ રિસર્ચ પ્રોફેસર ડૉ. વિજય તિરુવેંકટમે નોંધ્યું હતું.
આ પરમાણુઓ જીવંત પ્રણાલીઓમાં કામ કરશે કે કેમ તેનું મૂલ્યાંકન કરવા માટે, સંશોધકોએ LNCaP સેલ લાઇન પર તેમના સંયોજનોનું પરીક્ષણ કર્યું છે. જે માનવ પ્રોસ્ટેટ કેન્સર સેલ લાઇન છે, જે હજુ પણ હોર્મોન્સ પર પ્રતિક્રિયા કરે છે. પ્રારંભિક તબક્કાના પ્રોસ્ટેટ કેન્સર માટે પરીક્ષણ મોડેલ તરીકે નિયમિતપણે ઉપયોગમાં લેવાતા કોષોએ 5n ને મજબૂત પ્રતિક્રિયા આપી. ઓછી માત્રામાં પણ, સંયોજને કેન્સર કોષોના અસ્તિત્વને ઘટાડ્યું અને નવા ગાંઠો બનાવવાની અને ગુણાકાર કરવાની તેમની ક્ષમતાને નાટકીય રીતે અટકાવી હતી. સામાન્ય રીતે ઉપયોગમાં લેવાતી એન્ટિ-એન્ડ્રોજન દવા, બાયક્યુટામાઇડ સાથે સંયોજનમાં, 5n એ કેન્સર કોષોના અસ્તિત્વને ઘટાડવામાં છ ગણો સુધારો દર્શાવ્યો છે. વધારાના પ્રયોગો દર્શાવે છે કે આ દ્વિ સારવારથી નોંધપાત્ર DNA નુકસાન થયું છે. કેન્સર કોષો અને સક્રિય એપોપ્ટોસિસ, એક સ્વ-વિનાશ પદ્ધતિ જે કોષ તેની પોતાની અફર ખામીઓને ઓળખે છે. મહત્વપૂર્ણ રીતે, 5n એ સ્વસ્થ, બિન-કેન્સરગ્રસ્ત કોષો પ્રત્યે ઘણી ઓછી વિષાક્તતા દર્શાવી, જે સૂચવે છે કે તે પસંદગીયુક્ત રીતે કેન્સર કોષોને લક્ષ્ય બનાવે છે, જે સંભવિત ઉપચારમાં આડઅસરો ઘટાડવા માટે મહત્વપૂર્ણ છે.
કોઈપણ નવી દવા ક્લિનિક સુધી પહોંચે તે પહેલાં, તેને પરીક્ષણના સ્તરોમાંથી પસાર થવું આવશ્યક છે: પ્રાણી અભ્યાસ, સલામતી પરીક્ષણો અને માનવ સ્વયંસેવકો. આ પગલાંઓની અપેક્ષા રાખીને, ટીમે સિલિકો ADME (શોષણ, વિતરણ, ચયાપચય અને ઉત્સર્જન) વિશ્લેષણ હાથ ધર્યુ છે.
"અમે કોમ્પ્યુટેશનલ મોડેલોનો ઉપયોગ કરીને આગાહી કરી હતી કે તેમના સંયોજનો માનવ શરીરમાં કેવી રીતે વર્તે છે," શ્રીમતી શિવાંગી શર્મા, જે હાલમાં ટેક્સાસ A&M યુનિવર્સિટી, યુએસએમાં પીએચડી કરી રહી છે, તેમણે જણાવ્યું હતું. કમ્પ્યુટેશનલ મોડેલોનો ઉપયોગ કરીને સંયોજન 5n એ આ પરીક્ષણો સારા મૌખિક શોષણ, દવા જેવા ગુણધર્મો અને આશાસ્પદ સલામતી પ્રોફાઇલ સહિત અનુકૂળ ગુણધર્મો સાથે પાસ કર્યા હતા. વધુમાં, 5n તેના લક્ષ્યને કેવી રીતે જોડે છે તે પણ ગતિશીલ અભ્યાસોનો ઉપયોગ કરીને શોધવામાં આવ્યું હતું કે પરમાણુ TLK1ના વર્તનને વાસ્તવિક સમયમાં કેવી રીતે બદલે છે તે પદ્ધતિઓનો નકશો બનાવે છે. આ આંતરદૃષ્ટિ બ્લુપ્રિન્ટ્સ છે, જે સંયોજનના ભાવિ સંસ્કરણોની ડિઝાઇનને વધુ વિશિષ્ટતા અને શક્તિ સાથે માર્ગદર્શન આપે છે.
પ્રોસ્ટેટ કેન્સર દર વર્ષે લાખો લોકોનો ભોગ લેવાનું ચાલુ રાખતું હોવાથી, વધુ અસરકારક ઉપચારની જરૂરિયાત તાત્કાલિક છે. "થેરાપી પ્રતિકારમાં સામેલ મુખ્ય પ્રોટીનને લક્ષ્ય બનાવીને અને ચોકસાઈ અને હેતુ સાથે પરમાણુઓના નવા વર્ગને ડિઝાઇન કરીને, અમે કેન્સરના સૌથી પડકારજનક સ્વરૂપોમાંના એકની સારવાર માટે એક નવો માર્ગ ખોલ્યો છે," પ્રોફેસર કિરુબાકરણ કહે છે. આ સંશોધનની ભાવિ દિશામાં પ્રાણી મોડેલોમાં સલામતી અને અસરકારકતાનું મૂલ્યાંકન કરવા માટે વધુ પ્રીક્લિનિકલ અભ્યાસો સામેલ હશે, ત્યારબાદ સંભવિત ક્લિનિકલ ટ્રાયલ્સનો સમાવેશ થશે.
બાયોઓર્ગેનિક કેમિસ્ટ્રીમાં પ્રકાશિત આ અભ્યાસ, આંતરશાખાકીય સંશોધન કેન્સર ઉપચાર માટે નવા માપદંડો કેવી રીતે સ્થાપિત કરી શકે છે તેનું ઉદાહરણ આપે છે.
(रिलीज़ आईडी: 2132095)
आगंतुक पटल : 17